Podvýživa je jedným z prominentných a častých prejavov chronickej obštrukčnej choroby pľúc (CHOCHP), ktorá ovplyvňuje frekvenciu exacerbácií, respiračné parametre a kvalitu života pacientov. Cieľom štúdie je zhodnotiť nutričný stav pacientov s CHOCHP pomocou metód antropometrie a bioimpedancemetrie v komparatívnom aspekte. Vyšetrených bolo 60 pacientov s CHOCHP štádia I, II a III. Podľa výsledkov štúdie bol zistený pokles indexu telesnej hmotnosti (BMI) v CHOCHP štádia II a III v porovnaní s kontrolnou skupinou. K strate svalovej zložky alebo svalovej hmoty (TMB) dochádza už v I. štádiu CHOCHP, najvýraznejší pokles TMB bol zistený v III. štádiu ochorenia. Pri porovnaní týchto dvoch diagnostických metód neboli zistené signifikantné rozdiely v BMI a TMT vo všeobecnej skupine pacientov s CHOCHP a v rôznych štádiách ochorenia. Pri rozdelení vyšetrovaných do skupín s normálnym, nízkym a vysokým indexom telesnej hmotnosti boli zistené signifikantné rozdiely v TMT v skupine pacientov s BMI >25 kg/m2. V tejto skupine má metóda bioimpedancemetrie nižšie hodnoty TMT v porovnaní s metódou antropometrie. V súlade s tým možno bioelektrickú impedančnú metódu odporučiť na presnejšie posúdenie a včasnú diagnostiku proteín-energetickej malnutrície u pacientov s CHOCHP s BMI > 25 kg/m2.
chronická obštrukčná choroba pľúc
nutričné nedostatky
antropometrická metóda
bioimpedancemetrická metóda
1. Avdeev S. N. Chronická obštrukčná choroba pľúc ako systémové ochorenie // Pulmonológia. - 2007. - č.2.
2. Nevzorova V. A., Barkhatova D. A. Charakteristiky priebehu exacerbácie CHOCHP v závislosti od povahy patogénu a aktivity systémového zápalu // Bulletin of Physiology and Patology of Respiration. - 2006. - č. S 23. - C. 25-30.
3. Nevzorova V. A. Systémový zápal a stav kostrového svalstva pacientov s CHOCHP / V. A. Nevzorova, D. A. Barkhatova // Terapeut. arch. - 2008. - T. 80.
4. Nevzorova V. A. Obsah adipokínov (leptín a adipokín) v krvnom sére pri rôznom nutričnom stave pacientov s CHOCHP / V. A. Nevzorova, D. A. Barkhatova // Zborník z XVIII. Národného kongresu o respiračných chorobách. - Jekaterinburg, 2008.
5. Rudman D. Hodnotenie stavu výživy // Vnútorné choroby. - M.: Medicína, 1993. T. 2.
6. Bernard s., LeBlanc P. a kol.: Oslabenie periférnych svalov u pacientov s chronickou obštrukčnou chorobou pľúc // Am.J.Respir.Crit.Care. Med. -1998.
7. Globálna iniciatíva pre chronickú obštrukčnú chorobu pľúc (GOLD). Globálna stratégia diagnostiky, manažmentu a prevencie chronickej obštrukčnej choroby pľúc. Správa z workshopu NHLBI / WHO. Posledná aktualizácia 2008. www.goldcopd.org/.
8. Zloženie tela analýzou bioelektrickej impedancie v porovnaní s riedením deutéria a kožnými riasami a tropometriou u pacientov s chronickou obštrukčnou chorobou pľúc /A.M.W.J.Schols, E.F.M.Wouters, P.B.Soeters a kol. // Am.J.Clin.Nutr. - 1991.- Sv. 53.- S. 421-424.
9. Prevalencia a charakteristika nutričnej deplécie u pacientov so stabilnou CHOCHP vhodných na pľúcnu rehabitáciu / A.M.W.J.Schols, P.B.Soeters, M.C.Dingemans et al // Am.Rev.Respir.Dis. -1993. - sv. 147. - S. 1151-1156.
ÚvodVýživový stav odráža stav plastových a energetických zdrojov organizmu, úzko súvisí s procesmi systémového zápalu, oxidačného stresu a hormonálnej nerovnováhy. Podvýživa je jedným z najvýraznejších a najčastejších prejavov chronickej obštrukčnej choroby pľúc (CHOCHP), ktorá ovplyvňuje frekvenciu exacerbácií, respiračné parametre a kvalitu života. Zistilo sa, že výskyt nedostatku proteínovej energie zhoršuje priebeh základného ochorenia a zhoršuje jeho prognózu.
Antropometrické merania sú jednoduchou a cenovo dostupnou metódou, ktorá umožňuje pomocou výpočtových vzorcov posúdiť zloženie tela pacienta a dynamiku jeho zmien. Pomer plastov a energetických zdrojov možno opísať prostredníctvom dvoch hlavných zložiek: svalovej hmoty (TMB), ktorá zahŕňa svaly, kosti a ďalšie zložky a je indikátorom metabolizmu bielkovín, ako aj tukového tkaniva, nepriamo odrážajúceho energetický metabolizmus. Pri nutričných deficitoch u pacientov s CHOCHP dochádza k neúmernej strate rôznych zložiek tela, pri ktorej absencia výrazných zmien v telesnej hmotnosti pacienta môže maskovať deficit bielkovín pri zachovaní normálnej alebo trochu nadbytočnej tukovej zložky.
Metóda antropometrických meraní sa neodporúča starším pacientom, rovnako ako pri edematóznom syndróme, vzhľadom na neúmerné rozloženie tukového tkaniva a jeho prevládajúcu lokalizáciu v dutine brušnej. Alternatívnym alebo presnejším meraním kompozitnej štruktúry tela je bioelektrická impedančná metóda, založená na hodnotení rozloženia objemov vody, pri ktorej sa odhaduje elektrická vodivosť tkanív. Pri vykonávaní impedancemetrie je stanovenie telesného zloženia založené na väčšej vodivosti TMT v porovnaní s telesným tukom, čo súvisí s rozdielnym obsahom tekutín v týchto tkanivách.
Porovnanie informačného obsahu široko používaných metód hodnotenia nutričných deficitov pri CHOCHP určuje relevantnosť štúdie.
Účel štúdie:
Zhodnotiť stav nutričného stavu pacientov s CHOCHP metódami antropometrie a bioimpedancemetrie v komparatívnom aspekte.
Materiály a metódy:
Vyšetrili sme 60 pacientov s fenotypovými prejavmi európskej rasy, žijúcich v Prímorskom kraji viac ako 15 rokov vo veku 63 ± 12,1 rokov, ktorí boli liečení na pneumologickom oddelení Mestskej klinickej nemocnice č.1 a alergospiračnom centre vo Vladivostoku. v rokoch 2009-2010. s diagnózou CHOCHP (všeobecná skupina pacientov). Všetci pacienti boli informovaní o štúdii v plnom rozsahu a vyplnili informovaný súhlas. Kontrolnú skupinu tvorilo 10 zdravých dobrovoľníkov nefajčiarov, 8 mužov a 2 ženy vo veku 59 ± 10,7 rokov, ktorí neboli príbuzní hlavnej skupiny. Na diagnostiku štádia CHOCHP boli použité odporúčania medzinárodnej klasifikácie GOLD 2008. Všetci vyšetrení pacienti boli na základe ukazovateľov postbronchodilatačného testu FEV1 rozdelení do 3 skupín: skupina I - 20 pacientov s CHOCHP v štádiu I (FEV1 = 85 ± 1,3), skupina II - 20 osôb s CHOCHP štádia II (FEV1=65±1,8), skupina III - 20 osôb s CHOCHP štádia III (FEV1=40±1,5). Kritériá vylúčenia zo štúdie boli prítomnosť bronchiálnej astmy, infarktu myokardu, mŕtvice a iných závažných ochorení, zneužívanie alkoholu a drog, starší ľudia, ktorí nie sú schopní pochopiť ciele a ciele štúdie, odmietnutie pacientov zúčastniť sa na štúdium. Na posúdenie nutričných deficitov boli použité metódy antropometrických meraní a výpočtov BMI, TMT, ako aj bioimpedancemetria a stanovenie BMI, BFMT (beztuková hmotnosť, vyjadrená v %). Pri výpočte antropometrických parametrov TMT bola použitá metóda Durnin-Womersley (1972), ktorá je založená na hodnotení priemerného kožného tukového záhybu (SCF) posuvným meradlom, po ktorom nasleduje výpočet TMT podľa vzorca v závislosti na pohlaví, veku pacienta a BMI. Definícia BMI, ktorá umožňuje prvotne diagnostikovať stupeň podvýživy, bola určená vzorcom A. Keteleho: BMI = MT (kg) / výška (m 2).
Bioimpedansometria bola uskutočnená pomocou reoanalyzátora "Diamant" St. Petersburg. Získané výsledky boli spracované na IBM PC s operačným systémom Windows-XP pomocou programu Statistica 6.0 s výpočtom aritmetického priemeru (M), jeho chyby (± m) a relatívnej chyby (± m %). Štatistické spracovanie pri porovnávaní dvoch nezávislých skupín bolo uskutočnené pomocou neparametrického Mann-Whitneyho testu a stanovením signifikantných rozdielov medzi skupinami podľa tohto kritéria. Rozdiely medzi porovnávacími hodnotami boli uznané ako štatisticky významné na hladine významnosti p<0,05. Анализ взаимосвязей проводился непараметрическим методом корреляционного анализа Спирмена для ненормального распределения с вычислением ошибки коэффициента корреляции.
Výsledky výskumu
Hlavná skupina pacientov mala tieto antropometrické údaje: priemerná výška 172 ± 5,3 cm, priemerná hmotnosť 76,5 ± 5,5 kg. Index fajčiara (HCI) bol v priemere 33 ± 2,3, skúsenosť s fajčením bola 30 ± 3,3 rokov, čo naznačuje vysoký stupeň rizika spojeného s nikotínom. Analyzovali sme pomer BMI (body mass index) a TMB %, ako aj BJMT pomocou metód antropometrie a bioimpedancemetrie u pacientov s CHOCHP v závislosti od štádia ochorenia (tabuľka 1).
Tabuľka 1. Pomer BMI, TMT a FBMT u pacientov s CHOCHP
|
skupiny prieskumu |
Antropometrická metóda |
Bioimpedancemetrická metóda |
||
|
Ukazovatele |
Ukazovatele |
|||
|
Kontrolná skupina |
||||
|
Všeobecná skupina |
25,2 ± 0,4 * |
72,2 ± 1,3 * |
25,0 ± 0,6 * |
71,7 ± 0,7 * |
|
CHOCHP štádium I |
75,5 ± 1,1 * |
75,5 ± 0,4 * |
||
|
CHOCHP Ijaetapy |
24,3 ± 0,9 * # |
72,0 ± 1,6 * # |
23,8 ± 0,8* # |
71,65 ± 0,6 # |
|
CHOCHP štádium III |
19,9 ± 0,7 * #& |
64,6 ± 1,7 *#& |
19,4 ± 0,5 *#& |
64,2 ± 0,5 *#& |
Poznámka. Význam rozdielov (s<0,05): * - между группой контроля, общей группой и стадиями ХОБЛ, # - Významnosť rozdielov medzi CHOCHP štádia I a II, CHOCHP štádia I a III , & - medzi II a III štádiami CHOCHP.
Podľa prezentovaných výsledkov sú indexy BMI u pacientov s CHOCHP vo všeobecnej skupine nižšie ako v kontrolnej skupine v štúdii antropometriou aj bioimpedancemetriou. Analýza hodnôt BMI v závislosti od štádia CHOCHP ukázala, že v štádiu I ochorenia sa BMI v porovnaní s kontrolou nemení. K jej výraznému poklesu dochádza len v II. a III. štádiu CHOCHP (s<0,05). Несмотря на снижение показателей ИМТ по сравнению с контрольной группой, при всех стадиях ХОБЛ ИМТ находится в пределах референсных значений для нормальных показателей или превышает 20 кг/м 2 . Различий в значениях ИМТ, определенных как методом антропометрии, так и импедансометрии не установлено. Выяснено, что показатели ИМТ при II и III стадиях ХОБЛ достоверно ниже, чем при I стадии ХОБЛ (p<0,05), более того установлено наибольшее снижение показателей ИМТ при III стадии заболевания (p< 0,05).
Údaje charakterizujúce TMT vo všeobecnej skupine pacientov s CHOCHP, získané antropometriou a bioimpedancemetriou, sú v porovnaní s kontrolnou skupinou výrazne znížené (p<0,05).
Výsledky analýzy hodnôt TMT v závislosti od štádia CHOCHP ukázali, že na rozdiel od BMI k strate TMT dochádza už v I. štádiu CHOCHP. V štádiu CHOCHP I sú teda ukazovatele TMT nižšie v porovnaní s kontrolou (s<0,05). При II и III стадиях ХОБЛ значения ТМТ становятся еще меньше (p<0,05), достигая минимальных результатов при III стадии ХОБЛ (p=0,004). В последнем случае показатели ТМТ достоверно ниже результатов, полученных при исследовании пациентов с I и II стадий ХОБЛ (p<0,05). Во всех группах различий в данных, относящихся к ТМТ, в результате использования методов антропометрии и биоимпедансометрии не установлено.
Na rozdiel od BMI, ktorý je v referenčnom intervale, u zdravých ľudí (BMI 18,5-25 kg/m2) vo všetkých štádiách CHOCHP ukazovatele TMT v štádiu III ochorenia klesajú pod odporúčané hodnoty a klesajú pod 70 %.
Na základe hlavného cieľa našej štúdie a na základe výsledkov autorov, poukazujúcich na väčšiu senzitivitu metódy bioimpedancemetrie pri hodnotení nutričného stavu pacientov so známkami obezity a nerovnomerným rozložením tukového a svalového tkaniva, sme porovnali BMI a TMT v skupinách pacientov v závislosti od tela s indexom hmotnosti.
Za týmto účelom boli pacienti s CHOCHP rozdelení do troch skupín: skupina I - BMI od 20-25 kg/m2, skupina II - BMI< 20 кг/м 2 и III группа ИМТ >25 kg/m2. Výsledky štúdie sú uvedené v tabuľke 2.
Tabuľka 2. Indikátory IM, TMT, FJMT u pacientov s CHOCHP v závislosti od hodnôt BMI
|
Indikátor |
jagrueppan=20 |
IIskupinan=20 |
IIjaskupinan=20 |
|
BMI20- 25 |
BMI< 2 0 |
BMI>25 |
|
|
TMT (%), antropometrická metóda |
|||
|
BJMT (%), bioimpedancemetrická metóda |
Poznámka: Význam rozdielov (s<0,05): *- между ТМТ метода антропометрии и БЖМТ биоимпедансометрии у пациентов ХОБЛ.
Ako vyplýva z prezentovaných výsledkov, u pacientov s CHOCHP s BMI > 25 kg/m 2 boli zistené významné rozdiely medzi hodnotami TMT ako výsledok antropometrickej metódy a BJMT pomocou bioimpedancemetrie. V tejto skupine pacientov boli ukazovatele TMT významne vyššie ako ukazovatele FBMT a dosahovali 78,5 ± 1,25 a 64,5 ± 1,08 p<0,05 соответственно. Очевидно, что использование метода биоимпедансометрии в группе пациентов ХОБЛ с ИМТ>25 kg/m 2 má jasné výhody pre diagnostiku straty BJMT v porovnaní so štandardnými antropometrickými meraniami.
Diskusia o výsledkoch
CHOCHP je charakterizovaná stratou hmotnosti spojenou s nerovnováhou bielkovín a energie. V klinickej praxi sa pri zisťovaní nutričného stavu pacientov často obmedzuje len na výpočet BMI. V dôsledku toho sa zistilo, že BMI u pacientov s CHOCHP vo všeobecnej skupine je nižší ako v kontrolnej skupine, a to ako v štúdii antropometriou, tak aj bioimpedancemetriou. Analýza hodnôt BMI v závislosti od štádia CHOCHP ukázala, že v štádiu I ochorenia sa BMI v porovnaní s kontrolou nemení. K jeho výraznému poklesu dochádza len v II. a III. štádiu CHOCHP. Zároveň, bez ohľadu na štádium CHOCHP, sú hodnoty BMI v rámci referenčných hodnôt pre zdravých ľudí alebo presahujú 20 kg/m 2 . Definícia BMI preto nestačí na posúdenie stavu výživy pri CHOCHP. Na posúdenie zloženia tela je potrebné odlíšiť telesný tuk od čistej telesnej hmoty, pretože CHOCHP s normálnym alebo zvýšeným BMI je charakterizovaný úbytkom svalovej hmoty.
Podľa našej štúdie boli hodnoty TMT vo všeobecnej skupine pacientov s CHOCHP, hodnotené antropometriou a bioimpedancemetriou, významne znížené v porovnaní s kontrolnou skupinou (p<0,05). Анализ результатов измерения ТМТ в зависимости от стадии ХОБЛ показал, что в отличие от показателей ИМТ при I стадии заболевания ТМТ достоверно ниже по сравнению с контролем (p<0,05).
V štádiách II a III CHOCHP dochádza u pacientov k ešte výraznejšej strate proteínovej zložky telesnej hmotnosti. Dokazuje to významný pokles údajov charakterizujúcich TMT pri CHOCHP štádiách II a III v porovnaní so štádiom I ochorenia. Najnižšie hodnoty TMT boli zistené v štádiu CHOCHP III. Je potrebné venovať pozornosť skutočnosti, že pokles TMT vyjadrený pod odporúčané hodnoty v štádiu III CHOCHP. Inými slovami, naša štúdia preukázala pokročilú stratu TMT u pacientov s CHOCHP v porovnaní s BMI. Charakteristickým znakom našej vzorky je, že u všetkých pacientov s CHOCHP bez ohľadu na štádium je BMI v rámci odporúčaných hodnôt pre zdravú populáciu. Napriek tomu sme pri oboch metódach výskumu zaznamenali skutočný pokles TMT v štádiu III CHOCHP. Vzhľadom na najvýraznejšie zmeny v hodnotách BMI a TMT v štádiu III CHOCHP sa nám zdalo zaujímavé vykonať korelačnú analýzu medzi indexmi BMI, TMT a FEV1.
Vykonaná korelačná analýza preukázala absenciu signifikantných vzťahov medzi FEV1, diagnostickým ukazovateľom štádia CHOCHP a BMI, v metódach antropometrie a bioimpedancemetrie. Zároveň bola zistená priama korelácia priemernej sily medzi hodnotami TMT ako výsledok štúdia antropometrickej metódy a FEV1 (R=0,40+/-0,9; p<0,001) и прямая связь средней силы между данными БЖМТ в результате измерений методом биоимпедансометрии и ОФВ1 (R=0,55+/-0,9; p<0,0005).
Je zrejmé, že pri CHOCHP najviac trpí taký indikátor zloženej štruktúry tela, ako je TMT alebo BJMT. Bez ohľadu na prítomnosť alebo neprítomnosť príznakov hypoxémie, strata TMT priamo súvisí s progresiou CHOCHP a znížením rýchlosti dýchacej funkcie.
Na základe účelu štúdie sa ukazovatele TMT a BJMT diagnostikované pomocou metód antropometrie a bioimpedancemetrie významne nelíšia, tieto metódy však boli použité s BMI u pacientov, ktorí neboli rozdelení do skupín s normálnym, nízkym a vysokým indexom telesnej hmotnosti , čo je potrebné vziať do úvahy. Analyzovali sme porovnávacie charakteristiky TMT a BJMT ako výsledok aplikovaných metód pre rôzne ukazovatele BMI. Boli odhalené signifikantné rozdiely medzi TMT získaným antropometriou a BJMT, ako výsledok merania metódou bioimpedansometrie, s BMI > 25 kg/m 2 u pacientov s CHOCHP (p<0,05). Однако при ИМТ (20-25 кг/м 2), находящегося в пределах референсного значения для здоровых людей и при ИМТ<20кг/м 2 , достоверных различий не выявлено.
Je zrejmé, že metóda antropometrických meraní sa neodporúča pacientom s BMI > 25 kg/m 2 z dôvodu prevládajúcej koncentrácie tukového tkaniva v dutine brušnej, čo vedie k podhodnoteniu celkovej tukovej hmoty.
Metóda bioelektrickej impedancie umožňuje presnejšie stanoviť proteín-energetický deficit s prevládajúcim poklesom svalovej hmoty u pacientov s CHOCHP s BMI > 25 kg/m 2 .
závery
- CHOCHP je charakterizovaná rozvojom nutričných deficitov, ktorých fenotypovými prejavmi je úbytok svalovej hmoty, zaznamenaný aj pri normálnom indexe telesnej hmotnosti. Dochádza k úbytku čistej telesnej hmoty, svalovej zložky tela, už v I. štádiu CHOCHP, najvýraznejší pokles TMT bol zistený v III. štádiu ochorenia (p.<0,05).
- Na rozdiel od indexu telesnej hmotnosti má strata svalovej hmoty priamy vzťah so štádiom CHOCHP, čo dokazuje vykonaná korelačná analýza.
- Vo všeobecnej skupine pacientov, bez zohľadnenia ukazovateľov telesnej hmotnosti, sa pri porovnaní metód antropometrie a bioimpedancemetrie ukazovatele BMI a TMT výrazne nelíšia. Metóda bioelektrickej impedancie umožňuje presnejšie stanoviť proteín-energetický deficit s prevládajúcim poklesom svalovej hmoty u pacientov s CHOCHP s BMI > 25 kg/m 2 .
Recenzenti:
- Duizen I. V., doktor lekárskych vied, profesor Katedry všeobecnej a klinickej farmakológie VSMU, Vladivostok.
- Brodskaya T. A., doktor lekárskych vied, dekan Fakulty vyšších štúdií VSMU, Vladivostok.
Bibliografický odkaz
Burtseva E.V. ŠTÚDIA NUTRIČNÉHO STAVU PACIENTOV s CHOCHP METÓDAMI ANTROPOMETRIE A BIOIMPEDANSOMETRIE // Moderné problémy vedy a vzdelávania. - 2012. - č. 2.;URL: http://science-education.ru/ru/article/view?id=5912 (dátum prístupu: 01.02.2020). Dávame do pozornosti časopisy vydávané vydavateľstvom "Academy of Natural History"
A skutočne je. Preventívna medicína je jednou z hlavných oblastí práce moderného zdravotníctva. Aká je jeho nevýhoda? Preventívne opatrenia sú masívne a nezohľadňujú vlastnosti každého človeka. V súčasnosti je čoraz častejšie počuť „preventívnu medicínu“. V Rusku sa táto oblasť len začína rozvíjať a európski špecialisti ju aktívne rozvíjajú už niekoľko rokov. Preventívna medicína sa zaoberá každým človekom individuálne s prihliadnutím na jeho vlastnosti. Špecialista teda pracuje s každým pacientom podľa systému individuálneho prístupu, čo výrazne zvyšuje účinnosť preventívnych opatrení.
Program na hodnotenie funkčného stavu organizmu bol vyvinutý na štúdium hemostázy (komplexný biologický proces v tele, ktorý zabezpečuje jeho životaschopnosť) u pacientov starších ako 18 rokov.
V prvej fáze absolvujete krvný test, aby ste zistili svoj nutričný stav. Je potrebné dodržiavať Podľa výsledku vyšetrenia dietológ zostaví individuálny plán sledovania, nápravu zistených porušení.
Zloženie výskumu v rámci komplexného programu:
Nutričný stav základný - 3900 rubľov.
zahŕňa: AST, ALT, GGT, alkalickú fosfatázu, feritín, kreatinín, močovinu, kyselinu močovú, celkový proteín, albumín, celkový bilirubín, celkový cholesterol, triglyceridy, HDL-C, LDL-C, CRP, CPK, glykovaný hemoglobín, ionizovaný vápnik , vápnik všeobecne, sodík, draslík, chlór, kompletný krvný obraz, TSH, LDH
Catad_tema Chronické ochorenie obličiek - články
Poruchy nutričného stavu a význam nízkobielkovinovej diéty s využitím ketoanalógov esenciálnych aminokyselín v prevencii bielkovinovo-energetickej malnutrície u pacientov s chronickým ochorením obličiek
Yu.S. Milovanov, I.I. Alexandrova, I.A. Dobrosmyslov Prvá Moskovská štátna lekárska univerzita. Sechenov z Ministerstva zdravotníctva Ruska, Moskva
Cieľ. Zistiť možnosti tradičnej antropometrie a bioelektrickej impedančnej analýzy (BIA) pre včasnú diagnostiku porúch nutričného stavu u pacientov s CKD s glomerulonefritídou (GN) v predialyzačných štádiách a pravidelnej hemodialýze, identifikovať najvýznamnejšie faktory ich rozvoja a prevencie.
Materiál a metódy.Štúdia zahŕňala 180 pacientov s GN, vrátane 1BB s chronickou GN a 25 s GN so systémovými ochoreniami: 13 so systémovým lupus erythematosus (SLE) a 12 s rôznymi formami systémovej vaskulitídy. V závislosti od diagnózy a štádia KVO boli všetci pacienti zaradení do štúdie randomizovaní do 2 skupín. Prvú skupinu tvorilo 155 pacientov s chronickou GN. Skupina 2 zahŕňala 25 pacientov so systémovými ochoreniami (SLE, systémová vaskulitída). Vek pacientov sa pohyboval od 21 do 80 rokov (46,7 ± 10,8 rokov), 61 žien a 119 mužov. ,3 roky). Štádiá TOVP sú definované podľa kritérií NKF K/Boe n(2002), pričom GFR sa vypočítala pomocou vzorca ckd epi.
Výsledky. Zo všetkých 180 pacientov s ST-UL KVO boli poruchy nutričného stavu zistené u 33,9 % podľa tradičnej metódy a u 34,4 % pomocou VID. Zároveň sa zvýšila frekvencia porúch nutričného stavu v závislosti od stupňa zlyhania obličiek. u pacientov oboch skupín, ktorí dostávali nízkoproteínovú diétu (MLD) v kombinácii s ketoanalógmi esenciálnych aminokyselín (KD) najmenej 12 mesiacov pred začiatkom štúdie (n=39), žiadny z nich nemal poruchy nutričného stavu (metóda VID). Zároveň medzi pacientmi, ktorí dostávali MVL, ale bez použitia ketokyselín, boli poruchy nutričného stavu zistené v 1,2 % prípadov a medzi pacientmi, ktorí neobmedzovali bielkoviny v strave (n = 31) - vo viac ako 11 % prípadov. Medzi pacientmi 1. a 2. skupiny, ktorí dostávali MVL v kombinácii s ketokyselinami v štádiu pred dialýzou najmenej 12 mesiacov pred začiatkom dialyzačnej liečby, ^ = 39), počas prvého roka liečby pravidelnou HL, výrazne menej často ako u pacientov (n=61), ktorým neboli v preddialyzačnom období predpisované ketoanalógy esenciálnych aminokyselín, boli zaznamenané poruchy nutričného stavu (metóda VID).
Záver. Voľné KVO vyžadujú včasnú diagnostiku porúch nutričného stavu a pravidelné sledovanie, a to aj s pomocou VID. Použitie ketoanalógov esenciálnych aminokyselín pri použití MVL v štádiu pred dialýzou CVP umožňuje udržanie nutričného stavu pacientov s CVP.
Kľúčové slová. Epidemiológia, poruchy výživy, chronické ochorenie obličiek, hemodialýza, nízkobielkovinová diéta, ketoanalógy esenciálnych aminokyselín
Úvod
Jedným z naliehavých problémov nefrológie je zlepšenie kvality života a celkového „prežívania“ pacientov s chronickým ochorením obličiek (CKD), ktorého prevalencia vo svete neustále narastá.
Napriek tomu, že zavedenie metód renálnej substitučnej terapie (RRT) prispelo k zvýšeniu strednej dĺžky života pacientov s CKD, objavilo sa množstvo nových problémov, vrátane tých, ktoré sú spojené s frekvenciou porúch nutričného stavu, bielkovinovo-energie podvýživa (PEM), najmä u pacientov na pravidelnej hemodialýze (GD). Poruchy stavu výživy majú významnú prognostickú hodnotu, pretože majú významný vplyv na prežívanie a úroveň rehabilitácie týchto skupín pacientov. Zistilo sa, že úmrtnosť pacientov počas prvého roka dialyzačnej liečby bola 15 % u pacientov s normálnym indexom telesnej hmotnosti – integrálny ukazovateľ stavu výživy a 39 % u pacientov s indexom telesnej hmotnosti nižším ako 19 kg/ m2.
V súčasnosti sú antropometria a bioelektrická impedančná analýza (BIA) jednoduchými a dostupnými neinvazívnymi metódami na hodnotenie stupňa porúch nutričného stavu, a to aj u pacientov s edémami. Neexistujú však žiadne práce, v ktorých by sa pomocou antropometrie a bioelektrickej impedančnej analýzy porovnávalo zhodnotenie stavu nutričného stavu pacientov s CKD v preddialyzačných štádiách CKD a počas liečby s pravidelnou HD, ako aj štúdia rizikových faktorov pre rozvoj porúch výživy u týchto pacientov.
Mnohé štúdie ukázali, že obmedzenie dennej kvóty bielkovín v potravinách na 0,3-0,6 g/kg/deň zabraňuje hromadeniu toxických produktov, znižuje alebo odďaľuje nástup uremickej dyspepsie. Výsledky niekoľkých ďalších štúdií, vrátane známej štúdie MDRD (Modification of Diet in Renal Disease), však takýto jednoznačný záver nedávajú. Rozdiel vo výsledkoch je vysvetlený ťažkosťami v organizácii MBD, jej dodržiavaní najmä v masovom meradle a zároveň v zabezpečení dostatočného obsahu kalórií v potravinách (najmenej 35 kcal/kg/deň). Ako zlepšiť kontrolu MBD, compliance pacientov s CKD, je predmetom prebiehajúceho výskumu. Ciele štúdie zahŕňali:
1. Určite frekvenciu a stupeň porúch nutričného stavu pomocou antropometrie a bioelektrickej impedančnej analýzy (BIA).
2. Zhodnotiť úlohu nízkoproteínovej diéty (MBD) v kombinácii s užívaním ketoanalógov esenciálnych aminokyselín v prevencii porúch nutričného stavu u pacientov v preddialyzačnom štádiu CKD a následne na dialýze.
Materiál a metopy
Štúdia zahŕňala 180 pacientov s GN, medzi nimi 155 s chronickými a 25 s GN so systémovými ochoreniami: 13 so systémovým lupus erythematosus (SLE) a 12 s rôznymi formami systémovej vaskulitídy. (tab. 1).
Spomedzi 180 pacientov zahrnutých do štúdie bolo 80 diagnostikovaných v štádiu III-IV CKD (počiatočné a stredne ťažké CKD) a medzi 100 pacientmi - štádium UD CKD (závažné CKD - štádium dialýzy).
V závislosti od etiológie a štádia CKD boli všetci pacienti zaradení do štúdie randomizovaní do dvoch skupín. (tab. 2). Prvú skupinu tvorilo 155 pacientov s chronickou GN, z toho 22 so štádiom III CKD (GFR -30 -
59 ml / min / 1,73 m 2), 40 s CKD štádium IV (GFR -15-29 ml / min / 1,73 m 2) a 93< 10 мл/мин/1,73 м 2). В группу 2 включены 25 больных с системными заболеваниями: 10 больных ХБП III стадии, 8 - IV и 7 - УД-стадии. Для более точной оценки роли степени почечной недостаточности в развитии нутритивных нарушений больные III стадии обеих групп были разделены на 2 подгруппы: в подгруппу IIIA включены больные с СКФ 45-59 мл/ мин/1,73 м 2 , в ШБ - больных с СКФ 30-44 мл/мин/1,73 м 2 (tab. 2).
| Tabuľka 2. Rozdelenie pacientov v závislosti od štádia CKD | ||||
| Skupiny pacientov | CKD štádium III | CKD štádium IV (GFR 15-29 ml / min / 1,73 m 2) | Štádium CKD VD (GFR< 10 мл/мин/1,73 м 2) |
|
A (GFR 45-59 ml / min / 1,73 m 2) | B (GFR 30-44 ml / min / 1,73 m 2) |
|||
Počet pacientov |
||||
skupina 1 (CGN), n = 155 | ||||
skupina 2 (GN pri systémových ochoreniach), n = 25 | ||||
Vek pacientov sa pohyboval od 21 do 80 rokov (46,7 ± 10,8 roka), žien bolo 61, mužov 119 (ryža. jeden). Trvanie CKD od začiatku renálnej dysfunkcie bolo 3,5-7,1 roka (5,2 ± 1,3 roka).
Diagnóza GN bola stanovená podľa klinického obrazu, u 2/3 pacientov bola diagnóza potvrdená morfologicky pri intravitálnej biopsii obličky.
Všetci pacienti zaradení do skupiny 1 mali GN bez exacerbácie. U 120 pacientov sa pokles GFR a zvýšenie kreatinínu spojilo so zmenšením veľkosti obličiek rôzneho stupňa (zmenšenie).

Systémové ochorenia boli diagnostikované podľa kritérií prijatých pre každú nosologickú formu.
U pacientov z tejto skupiny bol pozorovaný rekurentný priebeh nefritídy, u niektorých pacientov (10 - SLE, 2 - mikroskopická polyarteritída, 2 - Wegenerova granulomatóza) v anamnéze exacerbácie, klinicky prebiehajúce ako rýchlo progresívna nefritída, ktorej úľava kortikosteroidy, vrátane vysokých dávok (pulzová terapia). Kritériom pre zaradenie pacientov so systémovými ochoreniami do štúdie bola absencia známok aktivity ochorenia počas sledovaného obdobia (hypokomplementémia, vysoký titer protilátok proti dvojvláknovej DNA, anticytoplazmatické protilátky – p- a c-ANCA).
CKD sa určuje podľa kritérií NKF K/DOQI (2002), pričom GFR sa vypočíta pomocou vzorca CKD EPI.
Okrem všeobecného klinického vyšetrenia pacientov na nefrologickom oddelení sa na vyriešenie úloh vykonali špeciálne štúdie. (tab. 3).

Na zistenie stupňa poruchy nutričného stavu u pacientov s CKD sme použili dve metódy (tab. 3):
|
Tabuľka 3 Špeciálne metódy výskumu |
|
|
Metódy hodnotenia porúch nutričného stavu |
Frekvencia štúdia |
|
Diagnostické metódy |
|
|
Tradičné: |
|
|
1. Metódy subjektívneho hodnotenia (opýtanie sa, oboznámenie sa s anamnézou - identifikácia charakteristických ťažkostí, etiologické faktory). |
1 krát / 3 mesiace |
|
2. Antropometrické: |
1 krát / 6 mesiacov |
|
3. Laboratórium: |
1 krát / 3 mesiace |
|
II. Inštrumentálne. |
1 krát / 6 mesiacov |
|
III. Príjem bielkovín a obsah kalórií v potravinách podľa troch denných stravovacích denníkov |
1 krát / 3 mesiace |
|
IV. Dotazník kvality života SF-36 |
|
2. Inštrumentálna metóda hodnotenia - stanovenie zloženia tela pacienta pomocou bioelektrickej impedančnej analýzy (BIA monitor, Tanita Company, USA). Získané antropometrické merania a výsledky
BIA bola doplnená o subjektívne celkové hodnotenie (opýtanie sa, oboznámenie sa s anamnézou - identifikácia charakteristických ťažkostí, etiologické faktory) a laboratórne štúdie (koncentrácia plazmatického albumínu, absolútny počet lymfocytov v periférnej krvi, hladina transferínu v krvi).
Pri hodnotení kvality života bol použitý dotazník SF-36 (Medical Outcomes Study Survey Short Form-36) vo vlastnej modifikácii, týkajúci sa rôznych aspektov stavu fyzického a duševného zdravia pacientov.
Pri výpočte prežitia sa ako konečný bod bral začiatok substitučnej liečby.
U všetkých 100 pacientov s CKD Vl-a^mi (eGFR< 10 мл/мин/ 1,73 м 2) использованы стандартный интермиттирующий low-flux-ГД или интермиттирующая гемодиафильтрация (ГДФ) в режиме реального времени (on line).
Štatistické spracovanie materiálu bolo realizované pomocou programu SPSS 12.0. Kritická hladina významnosti nulovej štatistickej hypotézy (o absencii rozdielov a vplyvov) sa rovnala 0,05. Na analýzu kvalitatívnych premenných bol použitý Pearsonov test x 2 alebo Fisherov test pre tabuľky 2 x 2. Na určenie sily vzťahu bola použitá Spearmanova dvojstranná korelačná analýza alebo Pearsonova dvojstranná korelačná analýza. Na identifikáciu faktorov spojených s rozvojom porúch nutričného stavu sa použila viacnásobná postupná logistická regresná analýza.
výsledky
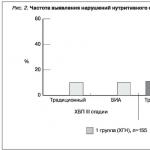
Zo všetkých 180 pacientov s CKD, III-VD štádia boli poruchy nutričného stavu (PEM) zistené u 33,9 % podľa tradičnej metódy a u 34,4 % pomocou BIA monitora. Frekvencia porúch nutričného stavu zároveň závisela od stupňa renálnej insuficiencie: medzi pacientmi s CKD s hladinou GFR 59-30 ml/min/1,73 m 1 %, kým medzi pacientmi s CKD s hladinou GFR 29– 15 ml/min/1,73 m (ryža. 2).
U pacientov 2. skupiny s CKD v rámci systémových ochorení s vysokou proteinúriou (> 1,5 g/deň), liečba kortikosteroidmi v anamnéze (> 6 mesiacov pred zaradením do štúdie) boli zaznamenané poruchy výživy aj pri miernom poklese v GFR (44-30 ml/min/1,73 m2). V 1. skupine boli zistené len u pacientov s CKD štádia IV podľa antropometrie aj BIA.
Výsledky skríningu odhalili rôzny počet pacientov s poruchami nutričného stavu v závislosti od použitej výskumnej metódy: tradičný – pre 59 pacientov (9 % v predialyzačných štádiách a 51 % na dialýze) a bioimpedančná analýza (BIA) – pre 64 pacientov (v uvedenom poradí 10 a 64 %. Pri objasňovaní príčiny nesúladu medzi výsledkami sa ukázalo, že u 5 pacientok (všetky ženy), u ktorých neboli tradičnou metódou zistené poruchy nutričného stavu, bol zaznamenaný stredne závažný edém trupu a končatín, ktorý viedol k tzv. nadhodnotenie výsledku antropometrických meraní a konečné zvýšenie výpočtu počtu bodov.
Metóda BIA teda umožňuje získať presnejšie ako tradičná metóda, ktorá zahŕňala antropometrické diagnostické parametre, výsledky stanovenia chudej a tukovej hmoty pacientov s edémom.
Medzi nami sledovanými pacientmi 1. a 2. skupiny (n = 39), ktorí dostávali MBD v kombinácii s liekom esenciálnych aminokyselín a ich ketoanalógov (EAA a CA) - Ketosteril® najmenej 12 mesiacov pred začiatkom liečby v štúdii nikto z nich nezaznamenal porušenie nutričného stavu (metóda BIA). Zároveň medzi pacientmi (n = 10), ktorí dostávali MBD, ale bez použitia EAC a CA, boli poruchy nutričného stavu zistené u 1,2 % a medzi pacientmi (n = 31), ktorí neobmedzovali bielkoviny v strave , viac ako 11 % prípadov (str< 0,05) (tab. 4).
|
Tabuľka 4. Frekvencia porúch nutričného stavu u pacientov so štádiom III-IV CKD v závislosti od |
|||
|
|
Diéty/počet pacientov (abs. počet; %) |
||
|
Skupiny pacientov |
MBD (0,6 g/kg/deň bielkovín) + ketoanalógy esenciálnych aminokyselín |
MBD (0,6 g/kg/deň bielkovín) |
|
|
skupina 1 (chronická GN), n = 62 |
|||
|
2. skupina (zápal obličiek pri systémových ochoreniach), |
|||
|
Celkom, n = 80 |
|||
|
* Prvé číslo zlomku je počet pacientov so zhoršeným nutričným stavom, druhé číslo je počet pacientov v podskupine; % z celkového počtu pacientov. |
|||
Pomocou korelačných koeficientov Pearsonových párov (Tabuľka 5) vplyv na zníženie indexu telesnej hmotnosti (BMI) ako integrálneho indikátora porúch nutričného stavu, nízky kalorický príjem (< 33 ккал/сут; связь прямая, сильная) (ryža. 3), závažnosť zlyhania obličiek (GFR< 30 мл/мин/1,73 м 2) (связь прямая, сильная), выраженности анемии (Hb < 9 г/дл; связь прямая, сильная), у больных 2-й группы также высокой протеинурии (>1,5 g/deň, spätná väzba, silný) (obr. 4) a trvanie liečby kortikosteroidmi (> 6 mesiacov, vzťah inverzný, silný). Kombinácia dvoch alebo viacerých týchto faktorov štatisticky významne zvýšila riziko vzniku porúch nutričného stavu.
|
Tabuľka 5. Faktory ovplyvňujúce pokles indexu telesnej hmotnosti (BMI) u pacientov v štádiu III-IV CKD (n = 80) 1 |
||||
|
|
Koeficient pary |
Pearsonove korelácie |
||
|
1. skupina (n = 62) |
2. skupina (n = 18) |
1. skupina (n=62) |
2. skupina (n = 18) |
|
|
príjem kalórií (< 33 ккал/кг/сут) |
||||
|
GFR< 30 (мл/мин/1,73 м 2) |
||||
|
Hb anémia< 9 (г/дл) |
||||
|
Proteinúria > 1,5 (g/deň) |
|
|||
|
Liečba kortikosteroidmi (trvanie > 6 mesiacov) |
|
|||

Vplyv nízkokalorickej diéty na chudnutie (o 3-5% za mesiac) je prezentovaný v ryža. 4. U pozorovaných pacientov s CKD v štádiu pred dialýzou zvyšovala pretrvávajúca proteinúria (> 1,5 g/deň) riziko úbytku hmotnosti (ryža. 4).

Zistila sa korešpondencia porušenia nutričného stavu so závažnosťou anémie (korelácia je priama, silná) (ryža. 6).

Medzi pacientmi s CKD štádiami III-IV oboch skupín, poruchy nutričného stavu (Tabuľka 6) sa signifikantne častejšie zistili u starších pacientov (> 65 rokov), s depresívnou náladou a intoleranciou na neslané, nekvasené jedlá. Títo pacienti mali často bakteriálne a vírusové infekcie, ktoré zhoršovali priebeh zlyhania obličiek a porúch výživy.
Pri viacnásobnom logistickom regresnom modelovaní bola signifikantne iba prítomnosť nízkokalorickej stravy bez ohľadu na vývoj porúch výživy (< 33 ккал/кг/сут) (Exp (B) = 6,2 (95 % ДИ - 2,25-16,8; р < 0,001) и СКФ < 30 (мл/мин/1,73 м 2) (Exp (B) = 1,07 (95% ДИ - 1,00-1,13; р = 0,049), у больных 2-й группы также высокой протеинурии (>1,5 g/deň) (Exp (B) = 2,05 (95 % CI - 1,2-2,5; p = 0,033) a liečba kortikosteroidmi (obdobie > 6 mesiacov) (Exp (B) = 2,01 (95 % CI - 1,0- 2,13; p = 0,035) pri úprave modelu na pohlavie a vek.
U nami sledovaných pacientov 1. a 2. skupiny, ktorí dostávali MBD v kombinácii s prípravkami EAA a KA v preddialyzačnom štádiu najmenej 12 mesiacov pred začiatkom dialyzačnej liečby (^ = 39), boli zaznamenané poruchy výživy. počas prvého roka liečby s pravidelným stavom HD (metóda BIA) výrazne menej často ako u pacientov (n = 61), ktorí nedostávali EAC a CA počas preddialýzy (tab. 7). U pacientov na programe HD v oboch skupinách boli tiež signifikantne častejšie zistené poruchy nutričného stavu (boli použité BIA + laboratórne metódy), u pacientov so syndrómom neadekvátnej dialýzy (Kt/V< 1,0; URR < 65 %), хронического воспаления (инфицированный сосудистый доступ, оппортунистические инфекции, вирусоносительство, гиперпродукция С-реактивного белка), а также при длительном использовании стандартного диализирующего раствора, содержащего уксусную кислоту (tab. 8) a rozvoj sekundárnej hyperparatyreózy (obr. 6).
Tabuľka 7. Frekvencia porúch nutričného stavu u pacientov s konečným štádiom CKD počas1 prvý rok liečby s pravidelnou HD v závislosti od stravy použitej v štádiu pred dialýzou (n=100)1 |
|||
Diéty v období pred dialýzou / počet pacientov (abs. počet; %) |
|||
Skupiny pacientov | MBD (0,6 g/kg/deň bielkovín) + keto analógy esenciálnych aminokyselín | MBD (0,6 g/kg/deň bielkovín) | Bez obmedzenia dennej kvóty bielkovín |
skupina 1 (chronická GN), n = 93 | |||
skupina 2 (nefritída pri systémových ochoreniach), n = 7 | |||
Celkom (n=100) | |||
* prvé číslo zlomku je počet pacientov s narušeným nutričným stavom, druhé je počet pacientov v podskupine; % z celkového počtu pacientov |
|||
U 12 nami pozorovaných pacientov dialýza koncentrátom s obsahom kyseliny octovej spôsobila nestabilitu hemodynamických parametrov (intradialyzačná hypotenzia), nauzeu, bolesti hlavy a anorexiu. Nahradenie všetkých 12 (popolových) tradičných koncentrátov pre HD koncentrátom, ktorý používa namiesto kyseliny octovej kyselinu chlorovodíkovú, umožnilo všetkým týmto pacientom vylúčiť intradialytickú hypotenziu a zlepšiť toleranciu HD procedúr, normalizovať chuť do jedla.
Podľa údajov uvedených v literatúre a výsledkov našej štúdie zvýšenie hladiny iPTH v krvnom obehu zvyšuje katabolizmus (rýchly úbytok hmotnosti na pozadí progresie metabolickej acidózy a hyperurikémie), exacerbáciu zlyhania obličiek. Zvýšenie koncentrácie iPTH s deficitom kalcitriolu a znížením aktivity bunkových receptorov vitamínu D (VDR) pri CKD vyvoláva vznik glomerulosklerózy a tubulointersticiálnej fibrózy.
Bola stanovená inverzná korelácia (r = (-)619; p< 0,01) между ИМТ (кг/м 2) и иПТГ (пг/мл) (ryža. 7).

Poruchy stavu výživy boli tiež významne častejšie u pacientov liečených intermitentnou nízkoprietokovou HD (x2 = 5,945, p = 0,01) v porovnaní s pacientmi liečenými intermitentnou hemodiafiltráciou (HDF) (tab. 9).
Pomocou HDF, vďaka vysokému prietoku krvi (300-400 ml/min) a intenzívnej ultrafiltrácii s hemodilúciou a automatickou volumetrickou kontrolou, bolo možné dosiahnuť uľahčené odstránenie prebytočnej tekutiny počas výkonu, zlepšenie stavu výživy (normalizácia svalovej hmoty a zvýšenie albumínu).
„U pacientov na programe HD, s využitím Coxovho regresného modelu, nepriaznivý vplyv hypoalbuminémie na riziko úmrtnosti z akejkoľvek príčiny (kardiovaskulárne komplikácie – CVK, infekcie a pod.), hospitalizácie pre CVC, nutnosť korekcie dialyzačného režimu ( pre každý koncový bod samostatne) bola stanovená) (obr. 7 a 8).

V porovnaní s pacientmi bez hypoalbuminémie medzi pacientmi s najzávažnejšou hypoalbuminémiou (< 30 г/л) установлен более высокий риск летальности (отношение шансов - ОШ 1,3; 95% доверительный интервал - ДИ 0,9-1,9), частоты госпитализаций по поводу ССО (ОШ - 2,18; ДИ - 1,76-2,70) и необходимости коррекции режима диализной терапии (ОШ - 5,46; ДИ - 3,38-8,822), причем ОШ отражало изменяющиеся во времени показатели альбумина и Kt/V.
Asociácia hypoalbuminémie so študovanými koncovými bodmi bola silnejšia so zvyšujúcou sa závažnosťou hypoalbuminémie. Na základe týchto výsledkov možno vyvodiť nasledujúci záver: úroveň poklesu albumínu je prediktorom zlej prognózy a komplikácií súvisiacich s CKD.
Hodnotenie kvality života v skupinách pacientov s zistenými poruchami nutričného stavu bolo realizované pomocou modifikovanej formy SF-36. Výsledky prieskumu pacientov sú uvedené v tab. 10.
Podľa našich údajov je prevalencia depresie a úzkosti, ktoré významne ovplyvňujú fyzickú aktivitu a sociálne vzťahy, 20 % u pacientov s preddialyzačnými štádiami CKD a zvyšuje sa na 50 % u dialyzovaných pacientov (p< 0,01). При этом некоторые составляющие качества жизни, такие,как общее самочувствие, утомляемость, склонность к депрессии и тревожность, усугублялись с увеличением диализного стажа.
Diskusia a závery
Hodnotili sme možnosti stanovenia telesného zloženia tradičnou metódou (ktorá zahŕňala subjektívne hodnotenie stavu pacienta, antropometrické a klinické parametre) v porovnaní s metódou BIA na včasnú diagnostiku porúch nutričného stavu u pacientov s CKD v preddialyzačných štádiách. a u dialyzovaných pacientov.
Tabuľka 9. Dynamika nutričného stavu pri liečbe HDF (metóda BIA) |
|||
Indikátor | Typ dialyzačnej terapie | ||
Prerušovaný HD s nízkym tokom | Prerušované HDF |
||
BMI, kg/m2 | |||
Percento tuku | |||
Percento svalovej hmoty | |||
Sérový albumín, g/l | |||
Sérový transferín, mg/dl | |||
Medzi 180 pacientmi boli poruchy nutričného stavu zistené u 3,1 % pacientov s počiatočným štádiom zlyhania obličiek (CKD štádium IIIB) bez rozdielov vo frekvencii porúch pri porovnávacom hodnotení tradičnou metódou antropometrie a bioelektrickej impedančnej analýzy. Výskyt porúch nutričného stavu sa zvyšoval priamo úmerne s nárastom renálneho zlyhania a závisel od diagnostickej metódy (tradičná antropometria alebo bioelektrická impedančná analýza), dosahoval 14,5 a 18,7 % u pacientov so štádiom IV CKD a 51 a 54 % u pacientov na dialýze. pacientov, resp.
Bioelektrická impedančná analýza podľa našich údajov poskytuje presnejšie informácie o pomere chudej a tukovej hmoty pacienta v porovnaní s tradičnou metódou zisťovania stavu výživy, najmä u pacientov s opuchmi. Metóda je vhodná na skríningové hodnotenie nutričného stavu tak v populácii pacientov v preddialyzačnej fáze liečby CKD, ako aj u dialyzovaných pacientov. Ak antropometrické merania trvali v priemere 40 ± 10,4 minúty, potom meranie pomocou BIA trvalo 2,5 ± 0,5 minúty.
Súčasťou diagnostiky nutričného stavu pomocou BIA u pacientov s CKD by malo byť aj pýtanie sa na ťažkosti pacienta, oboznámenie sa s anamnézou (identifikácia charakteristických ťažkostí, etiologických faktorov), stanovenie ukazovateľov viscerálnej syntézy bielkovín (obsah albumínu v krvnej plazme, transferínu a počtu lymfocytov v periférnej krvi).
Hodnotili sme vplyv rizikových faktorov spoločných pre CKD (typ diéty, vysoká proteinúria, dĺžka liečby kortikosteroidmi, depresia) a faktorov spojených s urémiou (sekundárna hyperparatyreóza, anémia, liečba programovou hemodialýzou) na vznik alebo progresiu porúch výživy. Zistilo sa to vo zvýšení ich frekvencie a závažnosti faktorov urémie a zvýšení ich úlohy pri CKD progredujúcej do Vr-n^rni.
Štúdia ukázala, že častejší PEI u dialyzovaných pacientov v porovnaní s obdobím pred dialýzou je spôsobený väčšou závažnosťou depresie, anorexiou, dodatočným zvýšením katabolizmu pri pravidelnej HD, ako aj vplyvom neúčinného dialyzačného režimu (pod dialyzačný syndróm).
Použitie MBD s využitím ketoanalógov esenciálnych aminokyselín v preddialyzačnom štádiu CKD umožňuje racionálne vyvážené stravovanie pacientov, predchádzanie vzniku porúch nutričného stavu pred dialýzou a priaznivo pôsobí neskôr na dialýze.
U pacientov s CKD štádiami III-VD je hypoalbuminémia úzko spojená s nárastom sprievodných ochorení (infekcií), hospitalizácií a rizika úmrtnosti. Pearsonove párové korelačné koeficienty odhalili inverznú koreláciu medzi hladinou C-reaktívneho proteínu akútnej fázy a albumínu v krvnom sére.
Syndróm chronického zápalu, diagnostikovaný u 18,8 % pacientov s PEU, bol spôsobený vplyvom infikovaného dialyzačného cievneho vstupu a oportúnnych infekcií (pneumónia, infekcia močových ciest a pod.). Významnú úlohu pri indukcii chronického zápalu a rozvoji porúch nutričného stavu zohrali aj sprievodné kardiovaskulárne ochorenia (ICHS, CMP), hypervolemická nadmerná hydratácia, syndróm acetátovej intolerancie a ťažká anémia.
Výsledky našej štúdie nám umožňujú rozšíriť naše chápanie epidemiológie porúch výživy u pacientov v štádiách CKD III-VD, identifikovať špecifické faktory, ktoré prispievajú k rozvoju a progresii CKD a PEU v tejto populácii. U pacientov s CKD boli v rámci systémových ochorení už zaznamenané poruchy výživy s miernym poklesom GFR (44-30 ml / min / 1,73 m 2), zatiaľ čo u pacientov s chronickým GN boli zaznamenané s výraznejším poklesom. v GFR (< 29 мл/мин/1,75 м 2). У всех больных ХБП в период включения в исследование отсутствовали признаки активности заболевания. Однако у подавляющего числа больных системными заболеваниями (СКВ, системные васкулиты), несмотря на развитие ХБП, сохранялась высокая протеинурия (>1,5 g/deň) a všetci mali v anamnéze exacerbácie ochorenia, počas ktorých pacienti dostávali kortikosteroidy dlhodobo (> 6 mesiacov), a to aj v ultravysokých dávkach. U pacientov s CKD v rámci systémových ochorení bola zistená súvislosť medzi rýchlym úbytkom hmotnosti a vysokou proteinúriou (inverzný vzťah, silný) a dĺžkou liečby kortikosteroidmi (priamy vzťah, silný). Zdá sa však, že úloha proteinúrie pri vzniku porúch výživy nebola obmedzená len na stratu bielkovín v moči. Existujú dôkazy, že proteinúria presahujúca 1 g/l, vyvolávajúca produkciu prozápalových cytokínov (TNF-a, IL-8) a rastových faktorov (transformujúci rastový faktor-p), chemokínov (monocytový chemoatraktant proteín-1, RANTES) tubulárneho epitelu a voľných kyslíkových radikálov, vedie k apoptóze tubulárneho epitelu s urýchlenou tvorbou tubulointersticiálnej fibrózy a progresiou renálneho zlyhania s vysokým rizikom rozvoja alebo exacerbácie porúch nutričného stavu. Hodnotenie úlohy proteinúrie ako hlavného faktora v progresii CKD (proteinurická remodelácia tubulointerstícia) však nebolo v rámci našej štúdie.
Výsledky našej štúdie a analýza literárnych údajov nám umožnili určiť princípy včasnej diagnostiky porúch nutričného stavu u sledovaných pacientov v štádiách CKD III-VD. (ryža. 9).

Všetci pacienti s CKD na nízkobielkovinovej diéte (0,6 g bielkovín/kg/deň) s nedostatočnou energetickou hodnotou potravy, vysokou proteinúriou (> 1,5 g/deň), dlhodobou (> 6 mesiacov) liečbou kortikosteroidmi.
Skríning na bielkovinovo-energetickú malnutríciu by sa mal vykonať v štádiu pred dialýzou u všetkých jedincov s CKD so sťažnosťami naznačujúcimi poruchy nutričného stavu:
Progresívne chudnutie;
depresie
zhoršenie arteriálnej hypertenzie, nevysvetliteľné iné príčiny;
rozvoj ťažkej anémie, ktorá nezodpovedá stupňu zlyhania obličiek (pokles erytropoézy môže byť spôsobený znížením syntézy bielkovín).
Je potrebné pravidelne monitorovať nutričný stav. Komplexné hodnotenie stavu výživy u pacientov s CKD je možné rýchlo vykonať pomocou BIA. Súčasne by sa mali analyzovať BMI, dynamika suchej hmotnosti, chudá a chudá telesná hmota, gastrointestinálne symptómy, čas dialýzy, laboratórne údaje (albumín a krvný transferín), miery hospitalizácie a riziko úmrtnosti na HD.
Použitie ketoanalógov esenciálnych aminokyselín pri použití MBD v predialyzačnej fáze CKD umožňuje udržať nutričný stav pacientov s CKD.
Literatúra
1. Milovanov Yu.S. Nefroprotektívna stratégia u pacientov s CKD v štádiu pred dialýzou. Vydavateľstvo: Lambert Academic Publishing. nemecko. 2011; 157 s.
2. Nikolaev A.Yu., Milovanov Yu.S. Liečba zlyhania obličiek. 2. vydanie. M. 2011. Vydavateľstvo: MIA. 58855 s.
3. Usmernenie klinickej praxe KDIGO na hodnotenie a manažment chronického ochorenia obličiek. 2013; (1):3.
4. Pokyny pre klinickú prax K/DOQI pre chronické ochorenie obličiek: hodnotenie, klasifikácia a stratifikácia. Am. J. Kidney Dis. 2002;39 (dodatok 1).
5. Chauveue P., Aparicio A. Prínosy vo výživových intervenciách u pacientov s CKD štádia 3-4. J Renálna výživa. 2001; 21 (1): 20-22.
6. Milovanov Yu.S. Chronické zlyhanie obličiek. V knihe „Racionálna farmakoterapia“ / ed. NA. Mukhina, L.V. Kozlovskaja, E.M. Shilov. Moskva: Litterra. 2006; 13:586-601.
7. Mukhin N.A., Tareeva I.E., Shilov E.M. Diagnostika a liečba ochorení obličiek. M.: GEOTAR-MED. 2002; 381 c.
8. Shutov E.V. Výživový stav u pacientov s chronickým zlyhaním obličiek (prehľad literatúry). Nephrol. vytočiť. 2008; 3-4 (10): 199-207.
9. Milovanov Yu.S., Nikolaev A.Yu., Lifshits N.L. Diagnostika a princípy liečby chronického zlyhania obličiek. Russ. med. časopis. 1997;23:7-11.
10. Smirnov A.V., Beresneva O.N., Parastaeva M.M. Účinnosť nízkoproteínových diét s použitím ketosterilu a sójového izolátu v priebehu experimentálneho zlyhania obličiek. Nephrol. vytočiť. 2006; 4(8): 344-349.
11. Ermolenko V.M., Kozlová T.A., Mikhailova N.A. Hodnota nízkoproteínovej diéty v spomalení progresie chronického zlyhania obličiek. Nephrol. a dialýzu. 2006; 4:310-320.
12. Kozlovskaja L.V., Milovanov Yu.S. Nutričný stav u pacientov s chronickým ochorením obličiek. Nefrológia: národné smernice / Ed. NA. Mukhin. Moskva: GEOTAR-Media. 2009; 203-210.
13. Kucher A.G., Kayukov I.G., Grigorieva N.D. Liečebná výživa v rôznych štádiách chronického ochorenia obličiek. Nephrol. vytočiť. 2007; 2(9):118-135
14. Milovanov Yu.S. Nízkobielkovinová diéta pri chronickom ochorení obličiek s renálnou insuficienciou v štádiu pred dialýzou: diétne zásady. Ter. archív. 2007; 6:39-44.
15. Garneata L., Mircescu G. Ketoanalógy u pacientov s CKD pred dialýzou: prehľad starých a nových údajov. XVI. medzinárodný kongres o výžive a metabolizme pri chorobách obličiek 2012, A31.
16. Študijná skupina Modification of Diet in Renal Disease (MDRD) (pripravil Levey AS, Adler S., Caggiula AW, Anglicko BK, Grerne T., Hunsicker LG, Kuser JW, Rogers NL, Teschan PE): Účinky diétneho proteínu obmedzenie na stredne závažné ochorenie obličiek v štúdii Modifikácie diéty v štúdii Renal Disease. Am. J. Soc. Nephrol. 1996;7:2616-26.
17. Milovanov Yu.S., Aleksandrova I.I., Milovanova L.Yu. Poruchy príjmu potravy pri dialýze Liečba akútneho a chronického zlyhania obličiek, diagnostika, liečba (praktické odporúčania). Wedge. nefrol. 2012; 2:22-31.
18. Fouque D. a kol. Výživa a chronické ochorenia obličiek. Kidney International 2011;80:348-357.
Kvantifikácia nutričného stavu pacienta je dôležitým klinickým parametrom a mala by sa vykonávať u každého pacienta.
Náklady na hospitalizáciu pacienta s normálnym nutričným stavom sú 1,5-5 krát nižšie ako náklady na pacienta s podvýživou. V tomto smere je najdôležitejšou úlohou lekára rozpoznať stavy podvýživy a adekvátne kontrolovať ich nápravu. Početné štúdie ukázali, že stav nedostatku proteínovej energie významne ovplyvňuje chorobnosť a mortalitu medzi pacientmi.
Obezitu a závažnú malnutríciu možno rozpoznať na základe anamnézy a klinického vyšetrenia, ale často sú pozorované menšie známky podvýživy, najmä v prítomnosti edému.
Kvantifikácia nutričného stavu umožňuje včas odhaliť život ohrozujúce poruchy a posúdiť pozitívne zmeny, keď sa začína zotavovanie. Objektívne merania stavu výživy korelujú s morbiditou a mortalitou. Žiadny z ukazovateľov kvantitatívneho hodnotenia stavu výživy však nemá jednoznačný prognostický význam pre konkrétneho pacienta bez zohľadnenia dynamiky zmien tohto ukazovateľa.
- Nutričný (výživový, trofologický) stav pacienta a indikácie na jeho posúdenie
V domácej literatúre neexistuje všeobecne akceptovaný termín na hodnotenie výživy pacienta. Rôzni autori používajú pojmy nutričný stav, nutričný stav, trofologický stav, bielkovinovo-energetický stav, nutričný stav. Pri hodnotení stavu výživy je najsprávnejšie používať pojem „výživový stav pacienta“, pretože odráža nutričnú aj metabolickú zložku stavu pacienta. Schopnosť včasnej diagnostiky malnutrície je nevyhnutná v praxi lekárov všetkých odborností, najmä pri práci s geriatrickým, gastroenterologickým, nefrologickým, endokrinným a chirurgickým kontinentom pacientov.
Nutričný stav by sa mal určiť v nasledujúcich situáciách:
- Pri diagnostike bielkovinovo-energetickej podvýživy.
- Pri sledovaní liečby bielkovinovo-energetickej podvýživy.
- Pri predpovedaní priebehu ochorenia a hodnotení rizika chirurgických a nebezpečných metód liečby (chemoterapia, rádioterapia atď.).
- Metódy hodnotenia stavu výživy
- Fyzikálne vyšetrenie
Fyzikálne vyšetrenie umožňuje lekárovi diagnostikovať obezitu aj bielkovinovo-energetickú malnutríciu, ako aj určiť deficit jednotlivých živín. Ak je u pacienta podozrenie na nedostatok živín, po vyšetrení je potrebné predpoklad potvrdiť laboratórnymi testami.
Odborníci WHO popisujú nasledujúce klinické príznaky proteínovo-energetickej podvýživy: vyčnievanie kostí kostry; strata elasticity kože; tenké, riedke, ľahko vytiahnuté vlasy; depigmentácia kože a vlasov; opuch; svalová slabosť; zníženie duševnej a fyzickej výkonnosti.
-
Živiny Poruchy a symptómy nedostatku Výsledky laboratórnych štúdií Voda Smäd, znížený kožný turgor, suché sliznice, cievny kolaps, duševná porucha Zvýšenie koncentrácie elektrolytov v krvnom sére, osmolarita krvného séra; zníženie celkového množstva vody v tele Kalórie (energia) Slabosť a nedostatok fyzickej aktivity, strata podkožného tuku, úbytok svalov, bradykardia Znížená telesná hmotnosť Proteín Psychomotorické zmeny, šedivenie, rednutie a vypadávanie vlasov, „šupinatá“ dermatitída, edém, ochabovanie svalov, hepatomegália, retardácia rastu Znížená OMP, sérové koncentrácie albumínu, transferínu, retinolu viazaného na proteíny; anémia; zníženie kreatinínu / rast, pomer močoviny a kreatinínu v moči; zvýšenie pomeru esenciálnych a neesenciálnych aminokyselín v krvnom sére Kyselina linolová Xeróza, deskvamácia, zhrubnutie stratum corneum, alopécia, stukovatenie pečene, oneskorené hojenie rán Zvýšenie pomeru triénových a tetraénových mastných kyselín v krvnom sére Vitamín A Xeróza očí a kože, xeroftalmia, tvorba Bytovho plaku, folikulárna hyperkeratóza, hypogeúzia, hyposmia Zníženie koncentrácie vitamínu A v krvnej plazme; zvýšenie trvania adaptácie na tmu vitamín D Rachitída a poruchy rastu u detí, osteomalácia u dospelých Zvýšená koncentrácia alkalickej fosfatázy v sére; zníženie koncentrácie 25-hydroxycholekalciferolu v krvnom sére vitamín E Anémia Zníženie koncentrácie tokoferolu v krvnej plazme, hemolýza erytrocytov Vitamín K Hemoragická diatéza Zvýšenie protrombínového času Vitamín C (kyselina askorbová) Skorbut, petechie, ekchymóza, perifolikulárne krvácanie, uvoľnenie a krvácanie ďasien (alebo strata zubov) Zníženie koncentrácie kyseliny askorbovej v krvnej plazme, počtu krvných doštičiek, hmotnosti plnej krvi a počtu leukocytov; zníženie koncentrácie kyseliny askorbovej v moči Tiamín (vitamín B1) Beriberi, bolesť a slabosť svalov, hyporeflexia, hyperestézia, tachykardia, kardiomegália, kongestívne zlyhanie srdca, encefalopatia Znížená aktivita tiamínpyrofosfátu a transketolázy obsiahnutých v erytrocytoch a zvýšené in vitro pôsobenie tiamínpyrofosfátu na ne; zníženie obsahu tiamínu v moči; zvýšené hladiny pyruvátu a ketoglutarátu v krvi Riboflavín (vitamín B2) Zaeda (alebo hranaté jazvy), cheilóza, Guntherova glositída, atrofia papíl jazyka, vaskularizácia rohovky, uhlová blefaritída, seborea, scrotal (vulválna) dermatitída Znížená aktivita EGR a zvýšený účinok flavínadeníndinukleotidu na aktivitu EGR in vitro; zníženie aktivity pyridoxal-fosfát oxidázy a zvýšenie účinku riboflavínu na ňu in vitro; zníženie koncentrácie riboflavínu v moči Niacín Pellagra, jasne červený a "ošúpaný" jazyk; atrofia papíl jazyka, trhliny jazyka, pelagroznyj dermatitída, hnačka, demencia Zníženie obsahu 1-metyl-nikotínamidu a pomeru 1-metyl-nikotínamidu a 2-pyridónu v moči
Poznámka: RBMS - bazálny metabolizmus; BUN, močovinový dusík v krvi; kreatinín/rast – pomer koncentrácie kreatinínu v dennom moči k rastu; EKG - elektrokardiogram; EGSUT - glutamín oxalooctová transamináza erytrocytov; EGR, erytrocytová glutatiónreduktáza; OMP - obvod svalov ramena; KZhST - kožný tukový záhyb nad tricepsom; RAI - rádioaktívny jód; Τ, trijódtyronín; Τ, tyroxín; TSH je hormón stimulujúci štítnu žľazu hypofýzy.
-
- Antropometrické merania a analýza zloženia tela
Antropometrické merania sú obzvlášť dôležité pri fyzickom vyšetrení. Antropometrické merania sú jednoduchou a cenovo dostupnou metódou, ktorá umožňuje pomocou výpočtových vzorcov posúdiť zloženie tela pacienta a dynamiku jeho zmien. Pri analýze získaných údajov je však potrebné pamätať na to, že tabuľkové údaje nie sú vždy vhodné pre konkrétnu osobu. Existujúce normy boli pôvodne vypočítané pre zdravých ľudí a nemusia byť pre pacienta vždy akceptované. Je správne porovnať zistené ukazovatele s údajmi toho istého pacienta v jeho priaznivom období.
- Telesná hmotnosť
Stanovenie telesnej hmotnosti (BW) je základom pre hodnotenie nutričného stavu.
Telesná hmotnosť sa zvyčajne porovnáva s ideálnou (odporúčanou) telesnou hmotnosťou. Za telesnú hmotnosť možno považovať telesnú hmotnosť vypočítanú podľa jedného z mnohých vzorcov a normogramov alebo telesnú hmotnosť, ktorá bola pre tohto pacienta v minulosti „najpohodlnejšia“. odporúčaná hmotnosť.
Edematózny syndróm môže ovplyvniť spoľahlivosť odhadu telesnej hmotnosti. Pri absencii edému slúži telesná hmotnosť vypočítaná ako percento ideálnej telesnej hmotnosti ako užitočný indikátor telesného tuku a svalovej hmoty. Ideálna telesná hmotnosť sa dá vypočítať zo štandardnej tabuľky výšky/hmotnosti.
Pri neúmernom úbytku rôznych zložiek tela môže absencia výrazných zmien v telesnej hmotnosti pacienta maskovať nedostatok bielkovín pri zachovaní normálnej alebo mierne nadbytočnej tukovej zložky (napríklad telesná hmotnosť vychudnutého pacienta, ktorý bol pôvodne obézny môže byť rovnaká alebo vyššia ako odporúčaná hodnota).
Pokles pomeru nameraná telesná hmotnosť / ideálna telesná hmotnosť na 80 % alebo menej zvyčajne signalizuje nedostatočnú bielkovinovo-energetickú diétu.
-
Limity telesnej hmotnosti (kg) Výška, cm Nízka Stredná vysoká MUŽI 157,5 58,11-60,84 59,47-64,01 62,65-68,10 160,0 59,02-61,74 60,38-64,92 63,56-69,46 162,6 59,93-62,65 61,29-65,83 64,47-70,82 165,1 60,84-63,56 62,20-67,19 65,38-72,64 167,6 61,74-64,47 63,11-68,55 66,28-74,46 170,2 62,65-65,83 64,47-69,92 67,65-71,73 172,7 63,56-67,19 65,83-71,28 69,01-78,09 175,3 64,47-68,55 67,19-72,64 70,37-79,90 177,8 65,38-69,92 68,55-74,00 71,73-81,72 180,3 66,28-71,28 69,92-75,36 73,09-83,54 182,9 67,65-72,64 71,28-77,18 74,46-85,35 185,4 69,01-74,46 72,64-79,00 76,27-87,17 188,0 70,37-76,27 74,46-80,81 78,09-89,44 190,5 71,73-78,09 75,82-82,63 79,90-91,71 193,04 73,55-79,90 77,63-84,90 82,17-93,98 ŽENY 147,3 46,31-50,39 49,49-54,93 53,57-59,47 149,9 46,76-51,30 50,39-55,84 54,48-60,84 152,4 47,22-52,21 51,30-57,20 55,39-62,20 154,9 48,12-53,57 52,21-58,57 56,75-63,56 157,5 49,03-54,93 53,57-59,93 58,11-64,92 160,0 50,39-56,30 54,93-61,29 59,47-66,74 162,6 51,76-57,66 56,30-62,65 60,84-68,55 165,1 53,12-59,02 57,66-64,01 62,20-70,37 167,6 54,48-60,38 59,02-65,38 63,56-72,19 170,18 55,84-61,74 60,38-66,74 64,92-74,00 172,72 57,20-63,11 61,74-68,10 66,28-75,82 175,26 58,57-64,47 63,11-69,46 67,65-77,18 177,8 59,93-65,83 64,47-70,82 69,01-78,54 180,34 61,29-67,19 65,83-72,19 70,37-79,90 182,88 62,65-68,55 67,19-73,55 71,73-81,27
-
- stavba tela
Hodnotenie zloženia tela je založené na koncepte extracelulárnej a intracelulárnej telesnej hmoty.
Bunkovú hmotu tvoria najmä viscerálne orgány a kostrové svaly. Hodnotenie bunkovej hmoty je založené na stanovení obsahu draslíka v organizme rôznymi, hlavne rádioizotopovými metódami. Extracelulárna hmota, ktorá plní prevažne transportnú funkciu, anatomicky zahŕňa krvnú plazmu, intersticiálnu tekutinu a tukové tkanivo a hodnotí sa stanovením výmenného sodíka. Vnútrobunková hmota teda odráža hlavne proteínovú zložku a extracelulárna hmota odráža tukovú zložku tela.
Pomer plastových a energetických zdrojov možno opísať prostredníctvom dvoch hlavných zložiek: takzvanej beztukovej alebo chudej telesnej hmoty (TMB), ktorá zahŕňa svaly, kosti a ďalšie zložky a je predovšetkým indikátorom metabolizmu bielkovín, a tukového tkaniva. ktorý nepriamo odráža energetický metabolizmus.
MT = TMT + tuková zložka.
Na posúdenie zloženia tela teda stačí vypočítať jednu z týchto hodnôt. Normálny obsah telesného tuku u mužov je 15-25%, u žien 18-30% z celkovej telesnej hmotnosti, aj keď tieto údaje sa môžu líšiť. Kostrový sval tvorí v priemere 30 % TMT, hmotnosť viscerálnych orgánov je 20 % a kostné tkanivo 7 %.
Pokles zásob telesného tuku je znakom výrazného deficitu energetickej zložky výživy.
- Metódy zisťovania zloženia tela
Na posúdenie obsahu tuku v tele sa zvyčajne používa metóda hodnotenia priemerného kožného tukového záhybu (antropometrické údaje). Existujú aj rôzne spôsoby výpočtu obsahu tukového tkaniva, ktoré sú založené na stanovení hustoty ľudského tela. Na základe rozdielu v hustote rôznych tkanív sa odhaduje tuková zložka.
Na posúdenie svalovej hmoty sa skúma vylučovanie kreatinínu alebo sa vykonáva bioimpedancemetria.
-
Hlavná metóda stanovenia obsahu telesného tuku je založená na hodnotení priemerného kožného tukového záhybu (SKF) posuvným meradlom pre niekoľko SKF (najčastejšie nad tricepsom, nad bicepsom, podlopatkovým a supraileálnym).
Posuvné meradlo je zariadenie, ktoré vám umožňuje merať QOL a má štandardný násobný kompresný pomer 10 mg/cm 3 . Výroba strmeňa je možná individuálne.
Pravidlá merania kožného tukového záhybu pomocou posuvného meradla.
- Antropometrické merania sa vykonávajú na nepracujúcom (nedominantnom) ramene a zodpovedajúcej polovici tela.
- Smer záhybov vytvorených počas merania sa musí zhodovať s ich prirodzeným smerom.
- Merania sa vykonávajú trikrát, hodnoty sa zaznamenávajú 2 sekundy po uvoľnení páčky zariadenia.
- Kožný tukový záhyb zachytí výskumník 2 prstami a potiahne ho späť asi o 1 cm.
- Merania na ramene sa vykonávajú s rukou voľne visiacou pozdĺž tela.
- Stred ramena: stred vzdialenosti medzi bodmi kĺbového spojenia ramena s akromiálnym výbežkom lopatky a olekranom lakťovej kosti (na tejto úrovni sa určuje aj obvod ramena).
- CVJ nad tricepsom sa určuje na úrovni stredu ramena, nad tricepsom (v strede zadnej plochy ramena), je umiestnený rovnobežne s pozdĺžnou osou končatiny.
- CVJ nad bicepsom sa určuje na úrovni stredu ramena, nad tricepsom (na prednej ploche ramena), je umiestnený rovnobežne s pozdĺžnou osou končatiny.
- Podlopatkový (podlopatkový) SCJ je definovaný 2 cm pod uhlom lopatky, zvyčajne sa nachádza v uhle 45° k horizontále.
- SIJ nad hrebeňom bedrovej kosti (supraileálny): určený priamo nad hrebeňom bedrovej kosti pozdĺž strednej axilárnej línie, zvyčajne umiestnený horizontálne alebo pod miernym uhlom.
- Antropometrické ukazovatele sa určujú v strednej tretine ramena nepracujúceho ramena. Ich proporcie umožňujú posúdiť pomer tkanív v celom tele.
- Zvyčajne sa merajú tricepsové kožné riasy (TSF) a obvod paže, z ktorých sa vypočíta obvod svalu paže (OMC).
Vypočítané hodnoty, ktoré charakterizujú hmotnosti svalov ramena a podkožného tukového tkaniva, korelujú s pomerne vysokou presnosťou s chudými (OMP) a tukovými (FAB) telesnými hmotnosťami, a teda s celkovými periférnymi rezervami. bielkovín a tukových zásob tela.
V priemere sú antropometrické ukazovatele zodpovedajúce 90-100% všeobecne akceptovaných ukazovateľov charakterizované ako normálne, 80-90% - zodpovedajúce miernemu stupňu podvýživy, 70-80% - miernemu stupňu a pod 70% - v ťažkej miere.
Základné antropometrické ukazovatele stavu výživy (podľa Heymsfield S.B. et al., 1982)
Indikátor Normy muži ženy Kožný záhyb nad tricepsom (KZhST), mm 12,5 16,5 Obvod ramena (OP), cm 26 25 Obvod svalu ramena (OMC), cm
\u003d OP - π × KZhST25,3 23,2 Plocha podkožného tukového tkaniva, cm 2
= KZhST×ΟΜΠ/2 – π×KZhST2/417 21 Plocha ramenného svalu, cm 2
= (ΟΠ – π × KZhST)2/4p51 43 Poznámka: sú uvedené priemerné hodnoty. Somatometrické ukazovatele sa líšia v závislosti od vekovej skupiny.
Imunologické ukazovatele hodnotenia stavu výživy.
- Komplexné metódy hodnotenia stavu výživy
Bolo vyvinutých veľké množstvo komplexných indexov a metód, ktoré umožňujú hodnotiť nutričný stav pacienta s rôznym stupňom spoľahlivosti. Všetky zahŕňajú kombináciu antropometrických, biochemických a imunologických parametrov.
- Zníženie telesnej hmotnosti o viac ako 10%.
- Zníženie celkovej bielkoviny v krvi pod 65 g/l.
- Znížený krvný albumín pod 35 g/l.
- Zníženie absolútneho počtu lymfocytov na menej ako 1800 na µl.
Subjektívne globálne hodnotenie podľa A. S. Detského a kol. (1987) zahŕňa klinické hodnotenie 5 parametrov:
- Strata hmotnosti za posledných 6 mesiacov
- Diétne zmeny (hodnotenie stravy).
- Gastrointestinálne príznaky (anorexia, nevoľnosť, vracanie, hnačka) trvajúce dlhšie ako 2 týždne.
- Funkčnosť (pokoj na lôžku alebo normálna fyzická aktivita).
- Aktivita choroby (stupeň metabolického stresu).
Súbežne s vyššie uvedenými štúdiami sa vykonáva subjektívne a fyzikálne vyšetrenie: strata podkožného tuku, úbytok svalov a prítomnosť edému.
Podľa vyššie uvedených ukazovateľov sú pacienti rozdelení do troch kategórií:
- S normálnym nutričným stavom.
- Pri miernom vyčerpaní.
- S ťažkým vyčerpaním.
Najčastejšie ide o bodovanie 8 rôznych markerov nutričného stavu. Medzi týmito indikátormi rôzni autori uvádzajú klinické hodnotenie, antropometrické a biochemické parametre, výsledky kožného testu s antigénom atď.
Hodnotí sa každý z ukazovateľov: 3 body - ak je v medziach normy, 2 body - ak zodpovedá ľahkému stupňu bielkovinovo-energetického deficitu, 1 bod - stredný, 0 bodov - ťažký. Súčet 1–8 bodov umožňuje diagnostikovať ľahkú bielkovinovo-energetickú malnutríciu, 9–16 bodov – strednú, 17–24 bodov – ťažkú. Celkové skóre 0 bodov znamená neprítomnosť podvýživy.
Podľa nariadenia Ministerstva zdravotníctva Ruskej federácie č.330 z 5. augusta 2003 sa hodnotenie stavu výživy vykonáva podľa ukazovateľov, ktorých súhrn charakterizuje nutričný stav pacienta a jeho potrebu. pre živiny:
- Antropometrické údaje: výška; telesná hmotnosť; index telesnej hmotnosti (BMI); obvod ramena; meranie kožného tukového záhybu tricepsu (TSF).
- Biochemické parametre: celkový proteín; bielko; transferín.
- Imunologické ukazovatele: celkový počet lymfocytov.
-
- Metódy zisťovania zloženia tela
- Telesná hmotnosť
- Fyzikálne vyšetrenie
![]() V minulom čísle nám bol určený základ – nutričná veda. Pre lepšie pochopenie témy musím uviesť niekoľko pojmov a faktov z pojmu - Výživový stav.
V minulom čísle nám bol určený základ – nutričná veda. Pre lepšie pochopenie témy musím uviesť niekoľko pojmov a faktov z pojmu - Výživový stav.
Nutričný stav- je komplex klinických, antropometrických a laboratórnych ukazovateľov charakterizujúcich kvantitatívny pomer svalovej a tukovej hmoty tela pacienta (pozri Bulletin vedecko-technického rozvoja č. 3 (31), 2010)
V poslednom čase začali do zdrojov informácií prenikať fakty o výraznom náraste ľudí s porušením tohto výživového stavu.
Malo by sa uznať, že medzi faktory predisponujúce k ochoreniam vnútorných orgánov podvýživa sú celkom bežné a významné. Dnes je tento typ podvýživy významný, ako napr nerovnováha stravy. Najčastejšie je v potravinách nedostatok niektorých aminokyselín, vitamínov, rastlinných tukov, mikroelementov, vlákniny a zároveň nadmerná konzumácia cholesterolu, živočíšnych tukov a rafinovaných produktov. Spomínaná podvýživa môže viesť k nutričnej nedostatočnosti, zmenám základných funkcií vnútorných orgánov, čo prispieva k vzniku patológia alebo exacerbácia chronických ochorení.
Správna výživa je teda základom života ľudského tela a je dôležitým faktorom pri zabezpečovaní odolnosti voči patologickým procesom rôzneho pôvodu.
nutričný stav - musíte jesť naplno
Podľa Výskumného ústavu výživy Ruskej akadémie lekárskych vied má 40 až 80% obyvateľov veľkých miest oslabenú imunitu, 30% Rusov má rôzne choroby tráviaceho systému, ktoré prudko zhoršujú procesy vstrebávania a trávenia. potravín [Lekárske noviny, 2.11.2011, „Rýchlejšie rásť spolu]:
- nedostatok vitamínu C v strave je pozorovaný u 70-100% populácie,
- nedostatok vitamínov B a kyseliny listovej - v 40-80%,
- nedostatok betakaroténu - 40-60%,
- nedostatok selénu - v 85-100%.
Prakticky zdravé telo by malo denne dostávať 12 vitamínov, 20 aminokyselín, celý komplex mikroelementov a minerálov.
Štúdie Výskumného ústavu výživy Ruskej akadémie lekárskych vied ukázali, že väčšina pacientov prijatých do nemocníc má výrazné poruchy. nutričný (potravinový) stav :
- 20% - vyčerpanie a podvýživa;
- 50% - poruchy metabolizmu tukov;
- až 90 % má príznaky hypo- a beriberi;
- viac ako 50 % má zmeny v imunitnom stave.
Analýza vykonaná Európskou asociáciou pre klinickú výživu a metabolizmus uvádza trofickú nedostatočnosť u pacientov:
- v chirurgii v 27-48%;
- v terapii u 46-59 %;
- v geriatrii v 26-57%;
- v ortopédii v 39-45%;
- v onkológii v 46-88%;
- v pneumológii v 33-63%;
- v gastroenterológii v 46-60%;
- medzi infekčnými pacientmi v 42-59%;
- s chronickým zlyhaním obličiek - 31-59%.
Pri miernom deficite živín (bielkoviny, tuky, uhľohydráty) sa v organizme v prípade choroby aktivujú kompenzačné mechanizmy, ktoré sú určené na ochranu životne dôležitých orgánov prerozdeľovaním plastových a energetických zdrojov:
- srdcový výdaj a kontraktilita myokardu sa znížia, môže sa vyvinúť atrofia a intersticiálny edém srdca;
- slabosť a atrofia dýchacích svalov vedie k poruche dýchacej funkcie a progresívnej dýchavičnosti, gastrointestinálne poškodenie sa prejavuje atrofiou sliznice a stratou klkov tenkého čreva, čo vedie k malabsorpčnému syndrómu;
- znižuje sa počet a funkčná schopnosť T-lymfocytov, zaznamenávajú sa zmeny vlastností B-lymfocytov, granulocytov, čo vedie k predĺženému hojeniu rán;
- trpí najmä funkcia hypotalamo-hypofyzárneho systému.
Tu je to, čo bolo napísané nedávno (úryvok)
Ošetrujúci lekár #6, 2009
Stav nutričného stavu moderných detí, možnosť jeho korekcie
N. L. Chernaya, G. V. Melekhova, L. N. Starunova, I. V. Ivanova, N. I. Ryzhova
Zo získaných údajov vyplynulo, že 26 % detí malo v tele nadbytočný podiel tukového tkaniva a zároveň len u 10 % detí sme podľa kaliperometrie zistili nárast podkožnej tukovej vrstvy. Pokles hrúbky podkožných tukových záhybov bol zistený u 39 % detí a len 11 % malo nedostatok tuku. 
Získané výsledky teda poukazujú na porušenie trofologického stavu u výrazne väčšieho počtu vyšetrených predškolákov ako podľa údajov antropometrie. Nie celkom porovnateľné výsledky získané metódami štúdia percenta tuku v tele a kaliperometriou sú spôsobené tým, že kaliperometria charakterizuje kvalitatívny stav rôznych častí ľudského tela. Predovšetkým zvýšenie podielu tukového tkaniva v tele dieťaťa je zákonite sprevádzané poklesom podielu chudej, takzvanej „štíhlej“ hmoty. Čistá (beztuková) telesná hmota pozostáva z kostrového a hladkého svalstva, hmoty viscerálnych orgánov, buniek pohybového aparátu. V rovnakom čase sa beztuková telesná hmota delí na extracelulárnu hmotu a bunkovú hmotu. Pri nedostatočnej výžive v počiatočnom štádiu sa v prvom rade spotrebuje bunková hmota a v 80% - kvôli svalom. Pokles svalového tonusu, ktorý sme zistili u takmer 70 % detí, je nepriamym potvrdením utrpenia bunkového kompartmentu tela.
Je známe, že pokles bunkovej hmoty je často sprevádzaný nárastom extracelulárnej, zvyčajne intersticiálnej tekutiny. Pokles tkanivového turgoru odhalený v našej štúdii u viac ako 60 % detí a zmenšenie hrúbky podkožných tukových záhybov je dôkazom zvýšenej hydrofilnosti telesných tkanív moderného dieťaťa (stav paratrofie).
Ukazuje sa teda, že prebytok na regáloch nie je ukazovateľom dobrej výživy
A na občerstvenie
Stupeň podvýživy sa hodnotí v súlade s odporúčaniami Európskej asociácie pre klinickú výživu a metabolizmus (ESPEN).
Bez ohľadu na príčinu sú klinické dôsledky podvýživy jednotné a zahŕňajú nasledujúce syndrómy:
- asteno-vegetatívny syndróm;
- svalová slabosť, znížená tolerancia cvičenia;
- imunodeficiencie, časté infekcie;
- dysbakterióza (alebo syndróm zvýšenej kontaminácie tenkého čreva);
- syndróm polyglandulárnej endokrinnej insuficiencie;
- tuková degenerácia pečene;
- strata libida u mužov, amenorea u žien;
- polyhypovitaminóza.
Zistilo sa, že telesná hmotnosť a úmrtnosť sú vzájomne prepojené parametre. Bolo dokázané, že úmrtnosť prudko stúpa s indexom telesnej hmotnosti nižším ako 19 kg/m2. Deficit telesnej hmotnosti 45–50 % je smrteľný [Russian Medical Journal, 29.06.2011].
------------
Záver: Povinné kompletná výživa.